产品概述
使用水溶性四唑盐WST-8作为显色物质的微生物比色法检测试剂盒。微生物通过能量代谢活动在细胞内生成NAD(P)H,WST-8在电子载体的作用下被NAD(P)H还原成水溶性的甲臜产物(橙色)。甲臜产物的生成量与微生物的能量代谢活性成正比例关系。因此,可以通过橙色的显色程度确认微生物的存活率和活性。
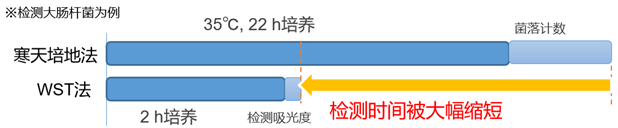
检测时间大幅缩短
传统的微生物活力检测一般采用克隆形成实验(Colony Formation Assay)或通过增殖造成的混浊等目视评价方法。这些方法需要的时间很长而且操作繁杂需要一定的熟练度才可以成功检测。而使用本试剂盒检测大肠杆菌时,相对于传统寒天培地法长达22小时的检测时间,本试剂盒仅需要8小时即可检测。(1 CFU/ml)
操作上更加简单快捷,培养后只需要加入试剂即可。检测时,在96孔板内准备好微生物悬浊液后加入试剂,在培养箱内通过微生物代谢活性开始显色。

大肠杆菌的增殖检测例
<检测步骤>
1.将大肠杆菌(NBRC3972)在TSBYE培养基中进行预培养。 2.用Mueller-Hinton(以下略称为MHB)配制成108 CFU/ml的大肠杆菌悬浊液,再用MHB制成10倍稀释系列悬浊液。 3.使用多通道移液器将不同菌体密度的大肠杆菌加入至96孔板中(每孔190 μl)。 4.使用多通道移液器向各孔中加入10 μl显色试剂。 5.为了防止蒸发和污染,用透明密封贴(PCR用等)贴在孔板上,置于酶标仪(VersaMax, 日本Molecular Devices)中。 6.用动力学测定模式(Kinetics)每隔15 min检测一次460 nm处吸光度直至24 h。(37℃)
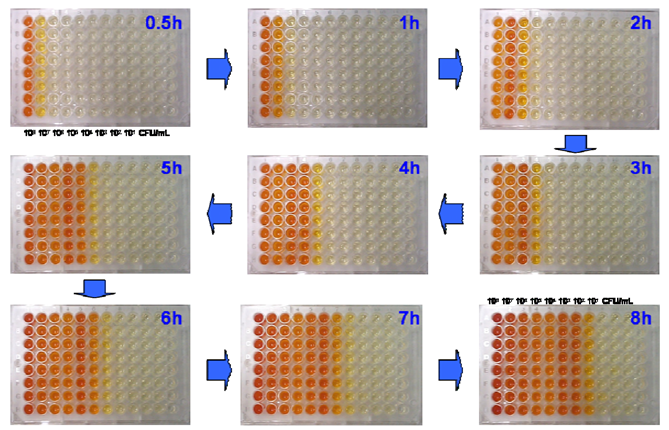
<检测结果和定量性的确认>
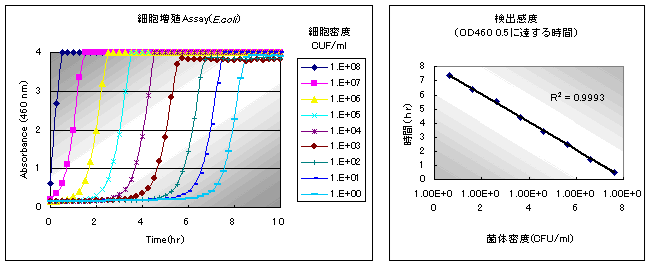
下图是随时间变化的大肠杆菌检测的结果。96孔板的最左列是高密度(约108 CFU/ml),
越往右密度越低,大约每隔1 h各列依次开始显色。
下图是图表化的大肠杆菌检测的结果。以“达到可以目视的吸光度值0.5所需要的时间(h)”为y轴,以各菌体密度(CFU/ml)为x轴作图。如下面的直线关系式,确认检测大肠杆菌的定量性。
y= -0.43Ln(x)+8.01
当x =1时,即1CFU/ml时,y =8.01。因此得知,1个微生物的检测大约需要8 h。也就是说,经过大约8 h培养后,吸光度如果没变化的话可以判定大肠杆菌阴性。
灵敏度更高
用容易分辨的“颜色”代替难以分辨的“浑浊度变化”
麦氏(McFarland)比浊法是通过菌液中的浑浊度来判断活菌数浓度的方法。而本试剂盒是通过颜色的变化检测活菌数的浓度。因肉眼的极限,使用比浊法无法判断的低浓度细菌活性,可以用灵敏度更高的本试剂盒进行检测。
下面是使用微生物定量法检测水溶性维他命之一的维他命B6的检测例。与传统的比浊法相比,可以在更短时间内更灵敏的进行定量。
维他命B6的微生物定量例
<检测步骤>
1.向96孔板的各孔中加入90 μl维他命定量用培养基。 2.向96孔板的各孔中加入90 μl标准溶液或样品溶液。 3.将10 μl配置好的各种需要维他命的菌种液和10 μl检测试剂加入孔中,30℃或37℃下培养一段时间。 4.将孔板置于酶标仪,使用终点(End Point)模式检测460 nm处吸光度。加入传统法的检测试剂,检测610 nm处的吸光度(浑浊度)。
使用微生物:Saccharomyces cerevisiae ATCC9080
使用培养基:维他命B6定量用基础培养基
培养温度:30℃
标准物质:吡哆醇盐酸盐
<检测结果和定量性的确认>
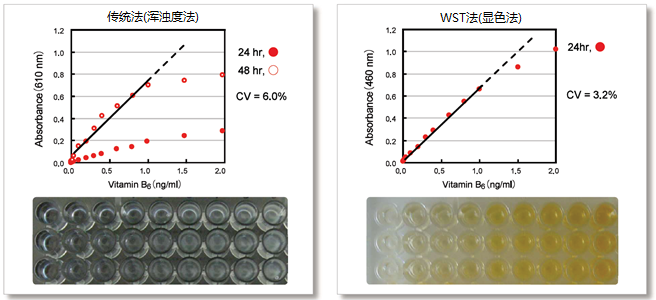
下图是本方法(WST法)和传统法的直线性的比较结果。本方法在培养24 h时,0.02~1 ng/ml的浓度范围内呈直线性。而传统法在培养24 h时,灵敏度仍达不到检测标准,需要将培养时间延长至48 h才能与本方法进行比较。
药物耐受性的实验例
<检测步骤>
1.将金黄葡萄菌(SA)和耐甲氧西林金huang色葡tao球菌(MRSA)分别播种至96孔板中。然后添加各浓度的抗生素。 2.在37℃下培养6 h,添加试剂后再培养2 h进行显色反应。
<检测结果和定量性的确认>
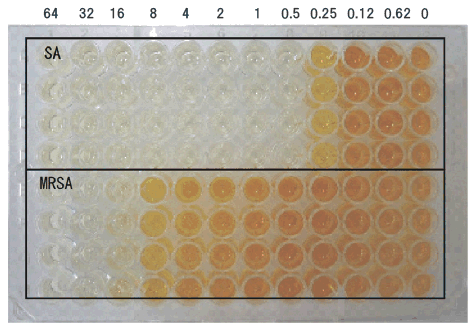
SA:Staphylococcus aureus
MRSA:Methicilin-resistant Staphylococcus aureus
传统方法对比
与传统抗菌性能实验(Spot-on-lawn法)的对比
抗菌性能检测的应用例
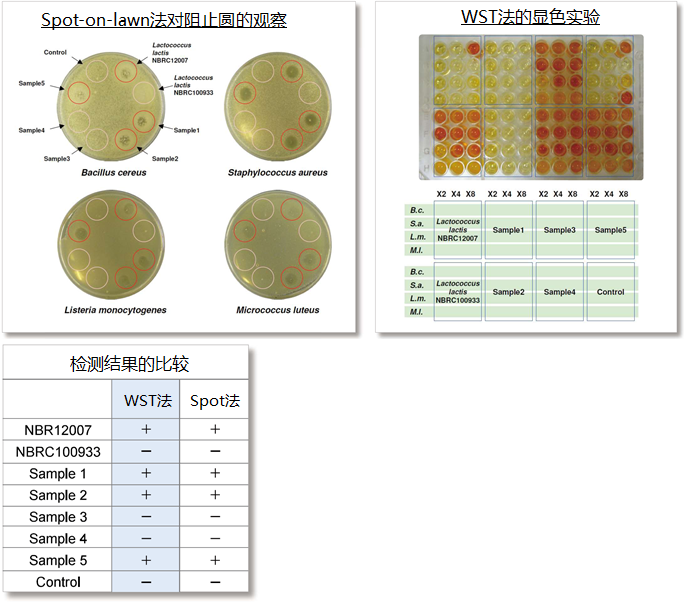
同时使用传统的Spot-on-lawn法(以下简称Spot法)和WST法进行抗菌性能对比实验。Spot法需要用目视的方法确认阻止圆的有无,而且检测所需的时间也更长。WST法的检测结果与传统法的结果相关性一致,而且可以在更短的时间内完成检测。下面是Spot法和WST法的抗菌性能检测实例。
用4种检定菌和待测样本共5种乳酸菌的培养上清液作为检测样本,筛选出具有产生抗菌能力的乳酸菌。
其中乳链菌肽(Nisin)生产菌之一的Lactobacillus lactis NBRC12007作为阳性对照,Lactobacillus lactis NBRC100933作为阴性对照。
为了分离出上清液中的抗菌物质,将乳酸菌培养上清液(pH 6.5-6.8)过滤并灭菌,然后用MHB培养基制备稀释系列,37℃培养6 h。
添加检测试剂之后, 37℃培养2 h。结果显示传统法与WST法相关性一致。
检测针对4种检定菌的24个供体的时候,Spot法需要12枚dish(每个dish8个检测点),检测时间需要20 h以上。而使用WST法检测时只需要1块96孔板,8 h左右即可完成检测。
显色原理
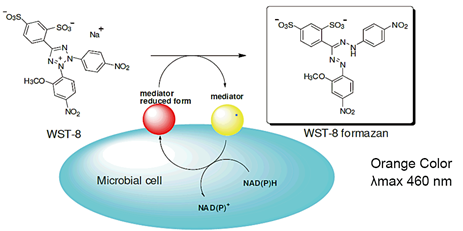
微生物通过能量代谢活动在细胞内生成NAD(P)H,WST-8在电子载体的作用下被NAD(P)H还原成水溶性的甲臜产物(橙色)。甲臜产物的生成量与微生物的能量代谢活性成正比例关系。因此,可以通过橙色的显色程度确认微生物的存活率和活性。
有检测实例的微生物
| 真菌(霉菌类):Mould | 真菌(酵母类):Yeast |
| Alternaria alternata NBR+B40:B56C31805 Aspergillus flavus NBRC4295 Aspergillus fumigatus NBRC33022 Aspergillus niger NBRC105649 Aspergillus terreus NBRC6346 Aspergillus ustus NBRC4128 Aureobasidium pullulans NBRC6353 Chaetomium globosum NBRC6347z Cladosporium cladosporioides NBRC6348 Exophiala dermatitidis NBRC6421 Paecilomyces variotii NBRC33284 Penicillium citrinum NBRC6352 Penicillium pinzophilum NBRC33285 Phoma citricarpa NBRC5287 Pseudallescheria boydii NBRC32229 Rhizopus oryzae NBRC31005 Sporothrix schenckii NBRC32961 Trichoderma virens NBRC6355 Trichophyton rubrum NBRC 5807 | Candida albicans ATCC90028 Candida albicans JCM 1542 Candida albicans SC5314 Candida krusei NBRC1395 Candida parapsilosis NBRC1396 Candida utilis Cryptococcus albidus NBRC0378 Cryptococcus neoformans ATCC66031 Saccharomyces cerevisiae NBRC2347 Trichosporon asahii NBRC103889 Trichosporon asahii M9459 Trichosporon asahii M9925 Zygosaccharomyces rouxi |
| 革兰氏阳性菌:Gram-positive | 格兰仕阴性菌:Gram-negative |
| Bacillus cereus Bacillus subtillis Corynebacterium glutamicum Enterococcus faecalis Enterococcus faecalis FSCC 146002 Lactobacillus casei Listeria monocytogenes Micrococcus luteus Staphylococcus aureus Staphylococcus aureus NBRC13276 Staphylococcus aureus ATCC 25923 Staphylococcus epidermidis Staphylococcus epidermidis ATCC 14990 Staphylococcus epidermidis FSCC 223011 Streptococcus mutans NCTC 10449 Streptococcus mutans UA 159 | Acetobacter sp. Acinetobacter baumannii ATCC 19606 Campylobacter concisus ATCC 33237 Enterobacter cloacae FSCC145003 Escherichia coli 1.1369 Escherichia coli ATCC 25922 Escherichia coli BW25113 Escherichia coli K-12 Fusobacterium nucleatum subsp. polymorphum JCM 12990 Klebsiella pneumoniae FSCC167002 Proteus mirablils Pseudomonas aeruginosa Pseudomonas aeruginosa NBRC13275 Pseudomonas aeruginosa ATCC 27853 Salmonella enteritidis Salmonella typhimurium Serratia marcescens Stenotrophomonas maltophilia ATCC 51331 Vivrio parahaemolyticus Yersinia enterocollica |
参考文献
| No. | 对象菌种 | 引用(链接) |
| 1) | <真菌(酵母)> | A. Azuma, N. Akiba and S. Minakuchi, "Hydrophilic surface modification of acrylic denture base material by silica coating and its influence on Candida albicans adherence", J. Med. Dent. Sci.., 2012, 59, (1), 1-7. |
| 2) | <革兰氏阴性菌> | H. Y. Oh, J. O. Lee and O. B. Kim, "Increase of organic solvent tolerance of Escherichia coli by the deletion of two regulator genes, fadR and marR", Appl. Microbiol. Biotechnol.., 2012, 96, (6), 1619-27. |
| 3) | <革兰氏阴性菌> | T. Nakayashiki, N. Saito, R. Takeuchi, H. Kadokura, K. Nakahigashi, B. L. Wanner and H. Mori, "The tRNA thiolation pathway modulates the intracellular redox state in Escherichia coli", J. Bacteriol.., 2013, 195, (9), 2039-49. |
| 4) | <革兰氏阳性菌> | S. He, P. Zhou, L. Wang, X. Xiong, Y. Zhang, Y. Deng and S. Wei, "Antibiotic-decorated titanium with enhanced antibacterial activity through adhesive polydopamine for dental/bone implant", J. R. Soc. Interface., 2014, 11, (95). |
| 5) | <真菌(霉菌)> | K. Z. Hein, H. Takahashi, T. Tsumori, Y. Yasui, Y. Nanjoh, T. Toga, Z. Wu, J. Grötzinger, S. Jung, J. Wehkamp, B. O. Schroeder, J. M. Schroeder and E. Morita, "Disulphide-reduced psoriasin is a human apoptosis-inducing broad-spectrum fungicide", Proc. Natl. Acad. Sci. U.S.A.., 2015, 112, (42), 13039-44. |
| 6) | <真菌(霉菌)> | S. Arai, T. Yoshino, T. Fujimura, S. Maruyama, T. Nakano, A. Mukuno, N. Sato and K. Katsuoka, "Mycostatic effect of recombinant dermcidin against Trichophyton rubrum and reduced dermcidin expression in the sweat of tinea pedis patients", J. Dermatol.., 2015, 42, (1), 70-6. |
| 7) | <革兰氏阳性菌> | T. Tsukatani, T. Kawaguchi, H. Suenaga, M. Shiga and T. Ikegami, "RAPID AND SIMPLE DETERMINATION OF MINIMUM BIOFILM ERADICATION CONCENTRATION BY A COLORIMETRIC MICROBIAL VIABILITY ASSAY BASED ON REDUCTION OF A WATER-TETRAZOLIUM SALT AND COMBINATED EFFECT OF ANTIBIOTICS AGAINST MICROBIAL BIOFILM", J Microbiol Biotechnol Food Sci.., 2016, 6, (1), 677. |
| 8) | <革兰氏阳性菌> | M. Hashimoto, H. Yanagiuchi, H. Kitagawa and Y. Honda, "Inhibitory Effect of Platinum Nanoparticles on Biofilm Formation of Oral Bacteria", Nano Biomed., 2017, 9, (2), 77-82. |
| 9) | <革兰氏阳性菌> | Z. Xu, X. Zhao, X. Chen, Z. Chen and Z. Xia, "Antimicrobial effect of gallium nitrate against bacteria encountered in burn wound infections", RSC Adv.., 2017, 7, 52266-52273. |
| 10) | <真菌(酵母)> | J. Nagao, T. Cho, M. Mitarai, K. Iohara, K. Hayama, S. Abe and Y. Tanaka, "Antifungal activity in vitro and in vivo of a salmon protamine peptide and its derived cyclic peptide against Candida albicans", FEMS Yeast Res.., 2017, 17, (1). |
| 11) | <真菌(霉菌)> | T. Ichikawa, C. Hirata, M. Takei, N. Tagami, H. Murasawa and R. Ikeda, "Cell surface hydrophobicity and colony morphology of Trichosporon asahii clinical isolates", Yeast., 2017, 34, (3), 129-137. |
| 12) | ・土壤微生物 | M. Kamitakahara, S. Takahashi, T. Yokoi, C. Inoue and K. Ioku, "Preparation of spherical porous hydroxyapatite granules as support materials for microorganisms", JCS Japan., 2018, 126, (9), 732-735. |
| 13) | <革兰氏阳性菌> | F. Boschetto, T. Adachi, S. Horiguchi, D. Fainozzi, F. Parmigiani, E. Marin, W. Zhu, B. McEntire, T. Yamamoto, N. Kanamura, O. Mazda, E. Ohgitani and G. Pezzotti, "Monitoring metabolic reactions in Staphylococcus epidermidis exposed to silicon nitride using in situ time-lapse Raman spectroscopy", J Biomed Opt.., 2018,(5), 1-10. |
| 14) | <革兰氏阴性菌> | T. Nambu, D. Wang, C. Mashimo, H. Maruyama, K. Kashiwagi, K. Yoshikawa, K. Yamamoto and T. Okinaga, "Nitric Oxide Donor Modulates a Multispecies Oral Bacterial Community-An In Vitro Study", Microorganisms., 2019, 7, (9), 353. |
常见问题Q&A
| Q: 是否可以用分光光度计的1 cm和0.25 cm比色皿进行检测? |
| A: 原则上可以。但是请注意,与使用96孔板相比,分光光度计检测时需要的试剂量更多,因此实际的检测次数有可能会低于试剂盒标注的检测次数。 |
| Q: 是否有丝状菌的检测实例? |
| A: Aspergillus(曲霉菌)属的麴菌(Koji-kin)有检测实例。 |
| Q: 在做细菌的增殖实验的时候,培养时间多长比较合适? |
| A: 微生物(细菌)的种类不同、细胞密度不同对应的培养时间也不一样。 例如,细胞密度为1×106 CFU/mL时,大约6小时左右开始融合。建议2~5.5 h范围内检测。 |
| Q: 可以检测专性厌氧菌吗? |
| A: 由于专性厌氧菌暴露于氧气下就会死亡,一般无法充分显色所以不能检测。 |
| Q: 目前有哪些微生物的检测实例? |
| A: 请参考本产品网站页面的“有检测实例的微生物”列表。 |